欧盟药品监管机构表示强生疫苗的益处胜过风险因为它审查了罕见的血块
能源公司概述了大型氢气项目的计划该计划将使用英国最大的电解槽
SpaceX增加了之前的一轮融资 使埃隆·马斯克的最后一次融资总额达到近12亿美元
截至3月底杭州市区二手房成交约11534套
要实现均衡发展首先就要弱化房地产的金融属性
Armadale合大街44号的物业的指导价格在1000万至1100万美元之间
位于25楼的Milsons Point子顶层公寓待售
Hurstville的新区正在将社区建设纳入虚拟领域
在即将进行的IPO中美国投资者如何购买Darktrace股票
杰夫·贝索斯的蓝色起源号发射并降落火箭新谢泼德以准备发射人员
这就是为什么2019年积压短期紧缩再次成为新闻的原因
社交媒体的Wallstreet Trapper提供了财务自由的机会
卡尔达诺因Coinbase效应而飙升但是会抛物线化吗
GeekMyTree在鲨鱼坦克出现后三年就消失了
丹·莫尔黑德的资产净值 对冲基金经理和加密货币投资者
摩根大通首席执行官杰米·戴蒙加入亿万富翁俱乐部
这些是高盛分析师所说的廉价全球股票
狗狗币突破10美分障碍 将目光投向20美分
Coinbase公开发行时Alexis Ohanian的资产净值
在IPOE合并之前SoFi值多少钱
GameStop可能成为下一个热门的NFT股票 这就是为什么
一些州所得税将于4月15日到期 大多数延期付款
两只新的贝莱德碳过渡ETF成为焦点
币安刚刚推出了特斯拉股票代币 它是如何工作的
强生疫苗暂停 链接到罕见的凝血障碍
尽管最近增长型股票有所回落但通过直接途径和SPAC进行的首次公开募股并不稀少
高油价是经济复苏的征兆
为什么在特朗普领导下美国国债升至7.8万亿美元
在即将进行的IPO中美国投资者如何购买Darktrace股票
内部管理的深刻变革才是首创置业备战十四五植根骨子里的变化
Hilco房地产宣布出售位于印第安纳波利斯的餐厅
Nicola Wealth房地产公司宣布了一项大型房地产收购计划
2021年房地产市场报告
Garbe Industrial房地产收购了Bitterfeld Wolfen的物流地块
Partners Group以超过10亿美元的价格出售工业房地产投资组合
Chime拒绝PPP贷款 其他企业替代方案
投资者的期权交易 基本知识
您听说过唯链吗 加密货币价格预测2021
在IPOE合并之前SoFi值多少钱
在伯克希尔灰色合并之前获得RAAC股票以讨价还价
房地产热潮将席卷马萨诸塞州
Fire Blocks开发人员购买住宅房地产
千禧一代准备接管房地产市场
Kitsilano's Golden Mile的半双工房屋以900万售出
在这个热门房地产市场上实现梦想家园的5个步骤
我用Amex商务白金卡购买了一辆新车,没什么大不了的
雪铁龙C5X是法国大型车的新品种
随着二手车价格上涨,个人财产税可能会增加
高尔夫球车制造商Club Car出售给底特律活塞队老板经营的投资公司
麦克莱恩县今年的汽车需求量已经上升
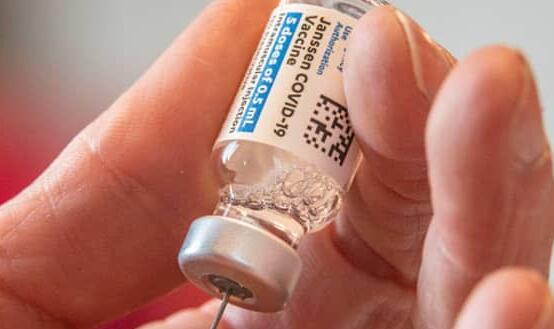
欧洲药品监管机构周三表示,在有极罕见的血液凝结报道后,它仍认为强生公司的当前局势疫苗的益处超过了产生副作用的风险。
不久前,美国食品药品监督管理局(US Food and Drug Administration)要求各州“出于谨慎考虑”暂时中止使用强生公司的疫苗,因为在超过680万剂注射中发现了6例血液凝固性疾病。
所有这六例病例均发生在美国,年龄在18至48岁之间,在接受注射后6到13天出现症状。FDA说,一名妇女死于血液凝固并发症,另一名妇女处于危急状态。
欧洲药品管理局表示,目前正在调查所有报告的病例,并将决定是否需要采取监管措施。
欧洲药品监管机构在一份声明中说:“ EMA目前正在加快这项评估,目前预计下周将发布建议。”
“尽管审查仍在进行中,但EMA仍然认为疫苗在预防当前局势方面的好处超过了产生副作用的风险。”
南非已经停止了注射疫苗的生产,而强生公司则表示将“主动推迟”将疫苗从上周开始运往欧洲。
该疫苗已于3月11日在欧盟获得批准,但尚未开始广泛使用。
FDA周二在与疾病控制和预防中心的联合声明中说:“目前,这些不良事件似乎极为罕见。”“ 当前局势疫苗的安全性是联邦政府的头等大事,我们非常认真地对待所有关于当前局势疫苗接种后健康问题的报道。”
上周,欧洲药品监管机构表示,它发现阿斯利康与牛津大学合作开发的当前局势疫苗与罕见的凝血问题之间可能存在联系。阿斯利康尚未获得在美国使用的授权
牛津-阿斯利康和强生的疫苗工作方式相似,均使用腺病毒,这是一种常见的局势,通常会引起轻微的感冒症状。
郑重声明:本网站所有信息仅供参考,不做交易和服务的根据,如自行使用本网资料发生偏差,本站概不负责,亦不负任何法律责任。如有侵权行为,请第一时间联系我们修改或删除,多谢。

















